الشيخوخة المبكرة 101 / الأسئلة الشائعة
ما هو مرض الشيخوخة المبكرة؟
متلازمة هتشينسون-جيلفورد بروجيريا (HGPS أو بروجيريا) هي مرض نادر للغاية ومميت ويؤدي إلى "الشيخوخة السريعة". اشتق اسمها من اللغة اليونانية وتعني "شيخوخة مبكرة". النوع الكلاسيكي هو متلازمة هتشينسون-جيلفورد بروجيريا، والتي سميت على اسم الأطباء الذين وصفوها لأول مرة: في عام 1886 بواسطة الدكتور جوناثان هتشينسون، وفي عام 1897 بواسطة الدكتور هاستينجز جيلفورد.[1]
ما مدى شيوع مرض الشيخوخة المبكرة؟
يصيب مرض الشيخوخة المبكرة حوالي 1 من كل 4 إلى 8 ملايين مولود جديد، ويصيب كلا الجنسين على حد سواء وجميع الأعراق. ويعاني واحد من كل 18 إلى 20 مليون فرد حي من مرض الشيخوخة المبكرة، ويقدر عدد الأطفال المصابين بمرض الشيخوخة المبكرة في جميع أنحاء العالم بنحو 400 طفل. ومنذ إنشاء مؤسسة أبحاث الشيخوخة المبكرة في عام 1999، تمكنا من العثور على الأطفال المصابين بمرض الشيخوخة المبكرة في 72 دولة وفي جميع القارات ومساعدتهم.[2]
ما هي مميزات مرض بروجيريا؟
على الرغم من أن الأطفال الذين يولدون عادة بمظهر صحي، إلا أن معظم الأطفال المصابين بالشيخوخة المبكرة يبدأون في إظهار خصائص الشيخوخة المبكرة خلال السنة الأولى من العمر. في بعض الأحيان تكون العلامات المبكرة للشيخوخة المبكرة هي شد أو انتفاخ الجلد في منطقة البطن و/أو الفخذ، والفشل في النمو (السقوط إلى ما دون منحنى النمو عند الأطفال). تشمل العلامات المبكرة الأخرى للشيخوخة المبكرة فقدان الدهون والشعر في الجسم، وتغيرات الجلد، وتقلصات المفاصل وبعض نتائج الأشعة السينية الواضحة. يصل الأطفال إلى أقصى ارتفاع في المتوسط 125 سم (49.21 بوصة) و 25 كجم (55.12 رطل). يتمتع الأطفال بمظهر متشابه بشكل ملحوظ على الرغم من اختلاف الخلفيات العرقية. مع تقدم الأطفال في السن، يصابون بتصلب الشرايين المتسارع وأمراض القلب والأوعية الدموية (القلب). هذا هو نفس تصلب الشرايين الذي يصيب عادة الأشخاص في الستينيات من عمرهم أو أكبر، لكنه يصيب المصابين بالشيخوخة المبكرة وبمعدل سريع.
ما هو سبب مرض الشيخوخة المبكرة؟
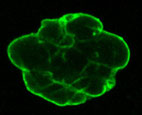
نواة خلية البروجيريا
قامت مجموعة من العلماء البارزين من اتحاد علم الوراثة التابع لمؤسسة PRF، بما في ذلك الدكتور فرانسيس كولينز، مدير المعهد الوطني لأبحاث الجينوم البشري آنذاك، بعزل جين بروجيريا. وفي إبريل 2003، أورد الاتحاد هذا الاكتشاف في المجلة العلمية الرائدة طبيعة.[3]
"عزل" ال الشيخوخة المبكرة جين يكون "إنجاز كبير لمجتمع البحث الطبي" وقال الدكتور فرانسيس كولينز، المؤلف الرئيسي لتقرير طفرة جين بروجيريا:لا يمنح هذا الاكتشاف الأمل للأطفال والأسر المتضررة من مرض الشيخوخة المبكرة فحسب، بل قد يلقي الضوء أيضًا على ظاهرة الشيخوخة وأمراض القلب والأوعية الدموية.
كشف اكتشاف جين بروجيريا أن مرض بروجيريا يحدث بسبب طفرة في الجين المسمى LMNA (تُنطق "لامين-أ"). LMNA ينتج الجين بروتين لامين أ، وهو جزء من الهيكل الهيكلي الذي يربط نواة الخلية معًا ويساعد في الحفاظ على صحة الخلايا. يسمى بروتين لامين أ غير الطبيعي الذي يسبب مرض الشيخوخة المبكرة بروجيرين. يؤدي هرمون البروجيرين إلى عدم استقرار الخلايا، مما يؤدي إلى عملية الشيخوخة المبكرة والمرض في مرض الشيخوخة المبكرة.
ما علاقة مرض الشيخوخة المبكرة بالشيخوخة؟
ولعل الدليل الأكثر إثارة للاهتمام فيما يتصل بعملية الشيخوخة هو اكتشاف أن بروتين البروجيرين يتواجد بتركيزات متزايدة في كل من الخلايا المصابة بمرض الشيخوخة المبكرة والخلايا الطبيعية مع تقدمنا في السن. وتتراكم البروتينات البروجيرينية في أجسامنا داخل خلايا الجهاز القلبي الوعائي بمعدل نحو 3% كل عام (وهو معدل أقل كثيراً من المعدل لدى الأطفال والشباب المصابين بمرض الشيخوخة المبكرة). وعلى هذا فإن فهم مرض الشيخوخة المبكرة يعد بفرص جديدة لفهم عملية الشيخوخة الطبيعية.
الأطفال المصابون بالشيخوخة المبكرة معرضون وراثيًا لأمراض القلب المبكرة والمتقدمة. تحدث الوفاة بشكل شبه حصري بسبب انتشار أمراض القلب هي السبب الرئيسي للوفاة في جميع أنحاء العالم.[4] وبالتالي، فمن الواضح أن هناك حاجة ماسة لإجراء أبحاث حول مرض الشيخوخة المبكرة. إن إيجاد علاج لمرض الشيخوخة المبكرة لن يساعد المصابين بهذا المرض فحسب، بل قد توفر أيضًا أدلة لعلاج ملايين البالغين المصابين بأمراض القلب والسكتة الدماغية مرتبط بعملية الشيخوخة الطبيعية.
هل تنتقل متلازمة الشيخوخة المبكرة من الأبوين إلى الأبناء؟
لا تنتقل متلازمة الشيخوخة المبكرة عادة بين أفراد العائلة. إن التغيير الجيني يحدث دائمًا تقريبًا بالصدفة وهو نادر للغاية. قد يصاب الأطفال المصابون بأنواع أخرى من متلازمات الشيخوخة المبكرة التي لا تنتمي إلى متلازمة الشيخوخة المبكرة بأمراض تنتقل بين أفراد العائلة. ومع ذلك، فإن متلازمة الشيخوخة المبكرة هي طفرة "جسمية سائدة متفرقة" - متفرقة لأنها تغيير جديد في تلك العائلة، ومهيمنة لأن نسخة واحدة فقط من الجين تحتاج إلى التغيير من أجل الإصابة بالمتلازمة. بالنسبة للآباء الذين لم ينجبو طفلًا مصابًا بالشيخوخة المبكرة، فإن الاحتمالات هي واحد من 4 إلى 8 ملايين. ولكن بالنسبة للآباء الذين ينجبون طفلًا مصابًا بالشيخوخة المبكرة، فإن احتمالات حدوث ذلك مرة أخرى لهؤلاء الآباء أعلى بكثير - حوالي 2-3%. لماذا الزيادة؟ يرجع هذا إلى حالة تسمى "الفسيفساء"، حيث يكون لدى أحد الوالدين الطفرة الجينية للشيخوخة المبكرة في نسبة صغيرة من خلاياه، لكنه لا يعاني من الشيخوخة المبكرة. تتوفر اختبارات ما قبل الولادة أثناء الحمل للبحث عن الطفرة الجينية للشيخوخة المبكرة في نسبة صغيرة من خلاياه، ولكن لا يعاني من الشيخوخة المبكرة. LMNA التغيير الجيني الذي يسبب HGPS في الجنين.
كيف يتم تشخيص مرض الشيخوخة المبكرة؟
بسبب اكتشاف جين بروجيريا التاريخي، لدينا طريقة علمية قاطعة لتشخيص الأطفال. يؤدي هذا إلى تشخيصات أكثر دقة وأسرع حتى يتمكنوا من تلقي الرعاية المناسبة. مؤسسة أبحاث الشيخوخة المبكرة لديها برنامج الاختبار التشخيصي يتم إجراء هذا الاختبار لتحديد التغير الجيني المحدد أو الطفرة في جين بروجيريا الذي يؤدي إلى متلازمة هودجكين. بعد التقييم السريري الأولي (بالنظر إلى مظهر الطفل والسجلات الطبية)، يتم اختبار عينة من دم الطفل للكشف عن بروجيريا. كما يتوفر الاختبار الجيني في بعض مرافق التشخيص الجيني. يُنصح دائمًا بالاستشارة الجينية المصاحبة.
هل يوجد علاج لمرض الشيخوخة المبكرة؟
نعم!تم صنع التاريخ في سبتمبر 2012عندما أظهرت نتائج أول تجربة سريرية لعقار بروجيريا أن عقار لونافارنيب، وهو مثبط فارنيسيل ترانسفيراز (أو FTI)، كان علاجًا فعالًا لمرض بروجيريا[5]وقد شهد جميع المشاركين في التجربة تحسنات كبيرة في زيادة الوزن، وبنية العظام، والأهم من ذلك، في نظام القلب والأوعية الدموية.
دراستان لاحقتان، واحدة من 2018 نُشرت في مجلة الجمعية الطبية الأمريكية (جاما)[6], وواحد من 2023 نُشرت في التوزيع[7], أثبتت أن لونافارنيب ساعد في إطالة البقاء على قيد الحياة لدى الأطفال المصابين بالشيخوخة المبكرة.
ال 2012 و 2018 أدت الدراسات إلى نتائج غير عادية 2020 وافقت إدارة الغذاء والدواء الأمريكية على عقار لونافارنيب، الذي يحمل الآن العلامة التجارية "زوكينفي"، كأول علاج على الإطلاق لمرض الشيخوخة المبكرة. وكان هذا الاعتماد بمثابة إنجاز مهم في مهمة PRF، حيث كان تتويجًا لثلاثة عشر عامًا من البحث السريري الذي تضمن أربع تجارب سريرية، حيث تم إحضار 96 طفلاً من 37 دولة إلى بوسطن للعلاج.
وبفضل هذا الإنجاز، انضمت بروجيريا إلى صفوف أقل من 5% من الأمراض النادرة التي لها علاج معتمد من إدارة الغذاء والدواء.
وبعد فترة وجيزة من موافقة إدارة الغذاء والدواء الأمريكية على استخدام لونافارنيب، وافقت وكالة الأدوية الأوروبية (EMA) على استخدام لونافارنيب في أوروبا في يوليو 2022، تلتها وزارة الصحة والعمل والرفاهية اليابانية (MHLW) في يناير 2024.
بدون لونافارنيب، يموت الأطفال بسبب تصلب الشرايين (قصور القلب أو السكتات الدماغية) في متوسط عمر 14.5 سنة [6] مع العلاج طويل الأمد بلوفارنيب، تتحسن صحة القلب والأوعية الدموية بشكل ملحوظ، لقد ثبت أن متوسط العمر المتوقع يزيد بمعدل 4.5 سنة7. وهذا يزيد بمقدار 30% عن متوسط العمر المتوقع، من 14.5 سنة إلى ما يقرب من 20 سنة!
مع ارتفاع أعمار الأطفال بسبب العلاج بلونفارنيب، يرى الأطباء أن تضيق الأبهر (تضييق صمام القلب الحرج) يمثل مشكلة لدى الأطفال الأكبر سنًا والشباب المصابين بمرض الشيخوخة المبكرة، وقد يكون من الممكن إجراء جراحة لإنقاذ حياتهم. وفي بعض الحالات، ساعدت الجراحة لإدخال صمامات قلب جديدة أو فتح الأوعية الدموية التي تغذي القلب (الدعامات) في تحسين صحة المرضى في المراحل المتأخرة من المرض.[8].
ما هي أحدث التطورات في أبحاث مرض الشيخوخة المبكرة؟
تشارك PRF بشكل كبير في تطوير ثلاثة مسارات علاجية أخرىوقد أظهرت كل منها مستويات متفاوتة من زيادة متوسط العمر المتوقع عند دراستها في نماذج الفئران المصابة بمرض الشيخوخة المبكرة - من 50% إلى 140% المذهل! وتتمثل أهدافنا في اكتشاف علاجات جديدة تعمل بشكل أفضل من عقار لونافارنيب وحده، وفي النهاية علاج مرض الشيخوخة المبكرة عن طريق تصحيح الطفرة الجينية. نحن نستهدف المرض على مستوى البروتين والحمض النووي الريبي والحمض النووي.
- تحرير قاعدة الحمض النووي:يهدف هذا المسار إلى تصحيح طفرة جين بروجيريا بشكل دائم على مستوى الحمض النووي.
في يناير 2021, مجلة العلوم طبيعة نُشرت نتائج رائدة توضح أن التحرير الجيني في نموذج الفأر لمرض بروجيريا أدى إلى تصحيح طفرة بروجيريا في العديد من الخلايا وتحسين العديد من أعراض المرض الرئيسية زيادة العمر الافتراضي للفئران بواسطة 140%[9]. ونحن بحاجة إلى دراسات ما قبل السريرية الإضافية للتحقيق في هذه النتائج، والتي نأمل أن تؤدي يومًا ما إلى تجربة سريرية.
قال الدكتور فرانسيس كولينز، الحاصل على درجة الدكتوراه: "إن رؤية هذه الاستجابة الدرامية في نموذج فأر بروجيريا الخاص بنا هو أحد أكثر التطورات العلاجية المثيرة التي شاركت فيها على مدار 40 عامًا كطبيب وعالم".
- العلاج بالحمض النووي الريبوزي:يهدف هذا المسار إلى إيقاف إنتاج البروجيرين عن طريق تصحيح الطفرة الجينية على مستوى الحمض النووي الريبي.
في مارس 2021ساهم PRF في دراستين رائدتين مثيرتين للغاية حول استخدام العلاجات القائمة على الحمض النووي الريبي، حيث تحاول كلتاهما منع قدرة الجسم على إنتاج البروجيرين على مستوى الحمض النووي الريبي. أظهرت إحدى الدراسات أن علاج فئران بروجيريا بعقار يسمى SRP2001 أدى إلى تقليل التعبير الضار للبروتين والرنا المرسال للبروجيرين في الشريان الأورطي، الشريان الرئيسي في الجسم، وكذلك في الأنسجة الأخرى. في نهاية الدراسة، أظهرت الفئران انخفاضًا في إنتاج البروجيرين. زيادة معدل البقاء على قيد الحياة لـ 62%[10].
وأظهرت الدراسة الأخرى انخفاضًا بنسبة 90 - 95% في الحمض النووي الريبي السام المنتج للبروجيجين في أنسجة مختلفة بعد العلاج بعقار يسمى LB143. وكان انخفاض بروتين البروجيجين أكثر فعالية في الكبد، مع تحسنات إضافية في القلب والشريان الأورطي.[11]يعد هذا التصحيح الجيني مؤقتًا، وبالتالي يلزم العلاج المستمر للحفاظ على التصحيح. - جزيء صغير (أدوية):يهدف هذا المسار إلى تقليل مستوى بروتين البروجيرين السام الذي يسبب مرض الشيخوخة المبكرة.
أظهر عقار يسمى بروجيرينين نتائج واعدة للغاية. ففي نموذج فأر مصاب بمرض الشيخوخة المبكرة، أدى البروجيرينين إلى زيادة وزن الجسم وإطالة العمر بمقدار 10 أسابيع، وهو إنجاز كبير، مقارنة بإطالة العمر بمقدار أسبوعين في الفئران المعالجة باللونوفارنيب.[12]يحرز مجال أبحاث مرض الشيخوخة المبكرة تقدمًا كبيرًا، وينمو باستمرار في النطاق والتعقيد مع استمرار البحث عن علاجات فعالة وعلاج. يقود الباحثون اللامعون والمتحمسون هذا المجال إلى اكتشافات وعلاجات جديدة تساعد الأطفال المصابين بمرض الشيخوخة المبكرة على العيش لفترة أطول وحياة أكثر صحة، بينما يقودون أيضًا الاكتشاف في أمراض القلب والشيخوخة. بالإضافة إلى استكشاف مسارات جديدة نحو العلاجات والعلاج، في مارس 2023، أعلنت PRF عن نتائج اكتشاف مؤشر حيوي لمرض الشيخوخة المبكرة، طريقة جديدة لقياس مستوى هرمون البروجيرينإن هذا الاختبار قادر على تحسين عملية التجارب السريرية من خلال توفير معلومات مبكرة حول فعالية العلاجات التي يتم اختبارها، كمقدمة لاختبارات سريرية أخرى مثل زيادة الوزن، والتغيرات الجلدية، وتقلص المفاصل ووظيفتها، وما إلى ذلك، وكلها تتطلب وقتًا أطول بكثير لتظهر. قد نتمكن الآن من فهم فوائد العلاج في وقت مبكر يصل إلى أربعة أشهر بعد بدء العلاج، أو إيقاف العلاج الذي قد لا يفيد المشارك في التجربة، لتجنب الآثار الجانبية غير الضرورية.[13]
كيف يساهم PRF في تعزيز البحث نحو علاج مستقبلي، ومساعدة الأطفال المصابين بالشيخوخة المبكرة اليوم؟
 مؤسسة أبحاث مرض الشيخوخة المبكرة تمويل البحوث الطبية تهدف إلى تطوير العلاجات والعلاج لمرض الشيخوخة المبكرة. كما تمتلك PRF أيضًا بنك الخلايا والأنسجة التي توفر المواد البيولوجية التي يحتاجها الباحثون لإجراء تجاربهم. بالإضافة إلى ذلك، تمتلك PRF قاعدة البيانات الطبية والبحثية – مجموعة مركزية من المعلومات الطبية من مرضى الشيخوخة المبكرة في جميع أنحاء العالم. يتم تحليل البيانات بدقة لمساعدتنا على فهم المزيد عن الشيخوخة المبكرة ووضع توصيات العلاج.
مؤسسة أبحاث مرض الشيخوخة المبكرة تمويل البحوث الطبية تهدف إلى تطوير العلاجات والعلاج لمرض الشيخوخة المبكرة. كما تمتلك PRF أيضًا بنك الخلايا والأنسجة التي توفر المواد البيولوجية التي يحتاجها الباحثون لإجراء تجاربهم. بالإضافة إلى ذلك، تمتلك PRF قاعدة البيانات الطبية والبحثية – مجموعة مركزية من المعلومات الطبية من مرضى الشيخوخة المبكرة في جميع أنحاء العالم. يتم تحليل البيانات بدقة لمساعدتنا على فهم المزيد عن الشيخوخة المبكرة ووضع توصيات العلاج.
للمساعدة في الإجابة على العديد من الأسئلة حول رعاية شخص مصاب بالشيخوخة المبكرة، نشرت PRF دليل البروجيريا يقدم هذا الدليل للعائلات والأطباء، من الحقائق الصحية الأساسية إلى توصيات الرعاية اليومية إلى إرشادات العلاج الشاملة، موردًا داعمًا للمساعدة في تحسين جودة الحياة للأشخاص المصابين بمرض الشيخوخة المبكرة في جميع أنحاء العالم. يتوفر أحدث إصدار من الدليل باللغات الإنجليزية والإسبانية واليابانية والبرتغالية والإيطالية والعربية والصينية. كما سيتوفر الدليل بلغات أخرى.
PRF تقود أيضًا التجارب السريرية لدواء بروجيريا وهي منظمة غير ربحية تعمل على اختبار العلاجات المحتملة، وقد قامت حتى الآن بتمويل وتنسيق أربع تجارب سريرية. لا تدخر PRF جهدًا في استكشاف الأدوية الواعدة التي ستقربنا من العلاج.
ماذا يمكنك أن تفعل لمساعدة الأطفال المصابين بالشيخوخة المبكرة؟
- تقديم مساهمة مالية. إن التبرعات مطلوبة دائمًا لمواصلة عمل PRF لإنقاذ الأرواح. لا يوجد تبرع صغير أو كبير جدًا - كل دولار له قيمته في سعينا لإيجاد العلاج! يتم قبول التبرعات عبر الإنترنت على يعطي.
- تبرع بوقتك. المتطوعون مهمون أيضًا لنجاح PRF. قم بإقامة حدث خاص مثل بيع المخبوزات أو غسيل السيارات؛ أو ترجمة المستندات للأسر؛ أو المساعدة في البريد - سنجد لك شيئًا لتفعله يناسب جدولك الزمني وموقعك ومواهبك! قم بزيارة موقعنا شارك الصفحة لرؤية كل الطرق التي يمكنك من خلالها المساعدة.
- تعرف على المزيد، ونشر الكلمة، وتواصل. هل تريد أن تتعلم المزيد عن العديد من البرامج والخدمات الحيوية التي تقدمها PRF للأطفال والشباب المصابين بالشيخوخة المبكرة؟ تفضل بزيارة موقعنا على الإنترنت موقع progeriaresearch.org
هل تعرف أحدا يمكنه المساعدة؟ أخبر أصدقاءك وعائلتك وزملاءك عن PRF والعمل المنقذ للحياة الذي نقوم به! في كثير من الأحيان، يكون الأشخاص أكثر ميلاً إلى التبرع لمنظمة ما إذا تلقوا توصية من شخص يعرفونه. لذا، ضع كلمة طيبة لنا وأخبر الجميع بمتابعتنا على إكس@progeria، "أعجب بنا" على فيسبوك، تحقق من صورنا على انستجرام @progeriaresearch، تعرف على مجتمع Progeria من خلال بعض فيديوهات اليوتيوب، واتصل بنا مباشرة على معلومات عنا.نحن نتطلع إلى التواصل معك!
معًا سنجد العلاج!
[1] تشمل متلازمات الشيخوخة المبكرة الأخرى متلازمة فيرنر، والمعروفة أيضًا باسم "الشيخوخة المبكرة للبالغين"، والتي لا تبدأ إلا في أواخر سنوات المراهقة، مع متوسط عمر يصل إلى الأربعينيات والخمسينيات.
[2] للحصول على خريطة توضح أماكن إقامة الأطفال الأحياء، يرجى الانتقال إلى https://www.progeriaresearch.org/meet-the-kids/.
[3] "الطفرات النقطية المتكررة الجديدة في اللامين أ تسبب متلازمة هتشينسون جيلفورد بروجيريا"، مجلة نيتشر، المجلد 423، 15 مايو 2003.
[4] إحصائيات جمعية القلب الأمريكية لأمراض القلب والسكتات الدماغية لعام 2021.
[5] جوردون إل بي، كلاينمان إم إي، وآخرون. تجربة سريرية لمثبط فارنيسيل ترانسفيراز في الأطفال المصابين بمتلازمة هتشينسون جيلفورد بروجيريا. Proc Natl Acad Sci US A. 9 أكتوبر 2012؛ 109(41):16666-71. doi: 10.1073/pnas.1202529109. Epub 24 سبتمبر 2012.
[6] جوردون إل بي، شابيل إتش، ماسارو جيه، وآخرون. العلاقة بين علاج لونافارنيب وعدم العلاج ومعدل الوفيات لدى المرضى المصابين بمتلازمة هتشينسون جيلفورد بروجيريا. JAMA. 2018؛ 319 (16): 1687-1695.
[7] جوردون، إل بي، نوريس، دبليو، هامرين، إس، وآخرون. بروجيرين البلازما في المرضى الذين يعانون من متلازمة هتشينسون جيلفورد بروجيريا: تطوير التحليل المناعي والتقييم السريري. التوزيع, 2023.
[8] جوردون إل بي، باسو إس، وآخرون. التدخل لعلاج تضيق الأبهر الحرج في متلازمة هتشينسون جيلفورد. الجبهة. القلب والأوعية الدموية. 11:1356010. دوى: 10.3389/fcvm.2024.1356010 (2024).
[9] كوبلان، إل دبليو، إردوس، إم آر، ويلسون، سي وآخرون. تحرير القاعدة في الجسم الحي ينقذ متلازمة هتشينسون-جيلفورد بروجيريا في الفئران. نيتشر 589، 608-614 (2021).
[10] Erdos, MR, Cabral, WA, Tavarez, UL et al. A Targeted antisense therapeutic approach for Hutchinson–Gilford progeria syndrome. Nat Med (2021). https://doi.org/10.1038/s41591-021-01274-0
[11] Puttaraju, M., Jackson, M., Klein, S. et al. Systematic detection identified therapeutic antisense oligonucleotides for Hutchinson–Gilford progeria syndrome. Nat Med (2021). https://doi.org/10.1038/s41591-021-01262-4
[12] كانج إس إم، ويون إم إتش، وآخرون. بروجيرينين، مثبط محسن لربط بروجيرين-لامين أ، يحسن من أنماط الشيخوخة المبكرة لمتلازمة هتشينسون-جيلفورد. بيول المجتمع. 4 يناير 2021؛ 4(1):5.
[13] جوردون، إل بي، نوريس، دبليو، هامرين، إس، وآخرون. بروجيرين البلازما في المرضى المصابين بمتلازمة هتشينسون جيلفورد بروجيريا: تطوير المقايسة المناعية والتقييم السريري. التوزيع, 2023

