Dieser allererste Antrag ist das Ergebnis von zwölf Jahren Forschungsdaten und vier von der PRF finanzierten klinischen Studien in Zusammenarbeit mit der Brown University und dem Boston Children's Hospital und wurde durch die mutigen Kinder und ihre Familien sowie IHNEN – der wunderbaren Spendergemeinschaft der PRF – ermöglicht.
Mehr zu dieser spannenden Neuigkeit können Sie hier lesen Hier.
Eiger BioPharmaceuticals wird fortlaufend vollständige Teile des Antrags zur Prüfung durch die FDA einreichen und plant, die Einreichung im ersten Quartal des neuen Jahres abzuschließen. Mit der Zulassung erhalten diese Kinder und jungen Erwachsenen in den USA und möglicherweise auch in anderen Ländern Zugang zu Lonafarnib – das ihnen nachweislich ein stärkeres Herz und ein längeres Leben beschert – auf Rezept statt über unsere klinischen Studien.
Was für ein positiver Abschluss des Jahres 2019 und ein starker Start ins neue Jahr! Wir haben unermüdlich daran gearbeitet, das Leben von Kindern und jungen Erwachsenen mit Progerie nachhaltig zu verbessern und dieser Beitrag bringt uns diesem Ziel näher.
DANKE EUCH ALLEN für die Unterstützung der Forschung, die uns nicht nur an diesen entscheidenden Punkt gebracht hat, sondern es uns auch ermöglicht, weiter an der Entdeckung neuer Medikamente zu arbeiten, mit denen diese außergewöhnlichen Kinder letztendlich geheilt werden können.
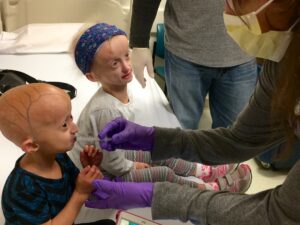
Zoey und Carly erhalten ihre Lonafarnib-Behandlung während ihres letzten klinischen Studienbesuchs in Boston.
