Essais cliniques et
Programme d'accès géré
Essais cliniques du médicament contre la progéria : contexte
 Les essais cliniques sur les médicaments contre la progéria représentent le meilleur espoir pour les enfants atteints de cette maladie. Ils permettent de tester des traitements potentiels qui pourraient leur permettre de vivre plus longtemps et en meilleure santé. Ces essais sont l'aboutissement d'années de recherche axées sur le médicament ou la combinaison de médicaments qui traiteront et guériront les enfants.
Les essais cliniques sur les médicaments contre la progéria représentent le meilleur espoir pour les enfants atteints de cette maladie. Ils permettent de tester des traitements potentiels qui pourraient leur permettre de vivre plus longtemps et en meilleure santé. Ces essais sont l'aboutissement d'années de recherche axées sur le médicament ou la combinaison de médicaments qui traiteront et guériront les enfants.
Depuis la création de la PRF en 1999, alors qu'il n'existait aucune ressource pour ces enfants, nous sommes passés d'une obscurité totale à la découverte de gènes, aux premiers essais cliniques sur la progéria, au tout premier traitement approuvé par la FDA, appelé lonafarnib, le tout à un rythme pratiquement inédit dans la communauté scientifique. Et tout en aidant cette poignée d'enfants, le lien entre la progéria et les maladies cardiaques courantes et le vieillissement a d'énormes implications pour nous tous.
Quelles sont les prochaines étapes en matière de traitements et de guérison ?
Lancement d'un nouvel essai clinique de médicament : le recrutement pour l'essai sur la progérinine a commencé !
PRF, en collaboration avec le sponsor de l'étude basé en Corée PRG Science & Technology (PRG S&T), a commencé le recrutement pour un tout nouvel essai clinique avec un médicament appelé Progerinin. Des preuves de laboratoire montrent que ce médicament, lorsqu'il est pris en association avec le lonafarnib, peut être plus efficace que le lonafarnib seul. PRF a financé les travaux de laboratoire qui ont conduit à la formation de PRG S&T et au développement de Progerinin. Les travaux préliminaires à l'essai ont commencé au Boston Children's Hospital, en prévision de l'inscription d'enfants du monde entier à cet essai dans les mois à venir. Nous sommes très enthousiastes à l'idée de lancer un nouvel essai avec un médicament aussi prometteur et avons hâte de partager plus de détails avec vous dès qu'ils seront disponibles.
Veuillez contacter Shelby Phillips pour en savoir plus sur le procès.
E-mail: sphillips@progeriaresearch.org
WhatsApp, Telegram, WeChat : 1-978-876-2407
Téléphone du bureau : 978-548-5308
La cofondatrice et directrice exécutive du PRF, Audrey Gordon, conclut en juin un accord avec le Dr Bum-Joon Park de PRG S&T pour avancer dans les travaux préliminaires au procès.
Thérapie par ARN : administration des médicaments L’étude de faisabilité est terminée !
Le PRF a fait les premiers pas avec les patients vers un essai clinique sur la thérapie par ARN – tellement excitant !
Contexte : En janvier 2021, nous avons signalé découvertes révolutionnaires dans le domaine thérapeutique de l'ARN, dans lequel cette thérapie production inhibée d'ARN codant pour la protéine responsable de la maladie de Progeria, la progérine. L'étude*, dirigée par le Dr Francis Collins, conseiller scientifique de la Maison Blanche et ancien directeur des National Institutes of Health (NIH), a révélé que des souris atteintes de Progeria traitées avec un médicament appelé SRP-2001 réduit l'expression de l'ARNm et des protéines nocives de la progérine dans les vaisseaux sanguins, ainsi que dans d'autres tissus. Les vaisseaux sanguins étaient plus forts et les souris ont montré une augmentation de la survie de plus de 60% par rapport aux souris non traitées. Ainsi, le travail avec cette thérapie prometteuse s'est poursuivi et nous avons pris la prochaine étape avec un Étude de faisabilité comme suit:
En règle générale, les thérapies à base d'ARN sont des liquides injectés par voie intraveineuse (directement dans la veine). Cependant, les personnes atteintes de progéria ne seraient pas en mesure de tolérer l'administration intraveineuse de la dose quotidienne requise. Ainsi, PRF a développé une système d'administration sous-cutanée grâce à quoi le liquide peut être injecté avec une petite aiguille sous la peau. Une étude de 6 mois a été réalisée au BCH pour déterminer la faisabilité de cette approche d'administration pour les personnes atteintes de progériaL'équipe a testé si l'administration d'une solution saline pouvait être confortablement injectée par voie sous-cutanée et quel système et site d'injection seraient les plus confortables. Une fois les données de cette étude analysées, nous serons Un pas de plus vers un essai clinique en thérapie génique!
*Erdos, MR, Cabral, WA, Tavarez, UL et al. Une approche thérapeutique antisens ciblée pour le syndrome de progéria de Hutchinson-Gilford. Médecine Nat (2021).
Que se passe-t-il AUJOURD'HUI avec les essais cliniques sur la progéria ?
L'essai le plus récent portait sur 2 médicaments : lonafarnib et un nouveau médicament, évérolimusLa phase 1, visant à déterminer le dosage sûr et approprié de l'évérolimus, a débuté en avril 2016 et s'est achevée avec succès en juin 2017. La phase 2, qui a testé l'efficacité de l'association de deux médicaments, a débuté en juillet 2017 et s'est achevée en avril 2022. Soixante enfants de 27 pays ont été inclus dans cette phase à deux médicaments !
L’évérolimus est une forme de rapamycine, un médicament qui pourrait être administré plus facilement aux enfants atteints de progéria, car il nécessite moins de prises de sang pour mesurer les concentrations du médicament. Alors que le lonafarnib peut bloquer le développement de la progérine toxique, la rapamycine semble permettre aux cellules d’éliminer plus rapidement la progérine. Ainsi, la rapamycine ciblant une voie différente de celle du lonafarnib, la combinaison pourrait s’avérer être un « coup double » contre la progéria – et, espérons-le, un meilleur traitement que le lonafarnib seul.
Nous sommes désormais entrés dans une période d’analyse des données et nous prévoyons de publier les résultats dans une revue scientifique à comité de lecture. Entre-temps, les participants à l’essai ont soit opté pour l’extension de l’essai en monothérapie, soit pour un autre programme d’accès. Quelle que soit la voie choisie, les participants continuent de recevoir du lonafarnib, le traitement de référence actuel.
Aperçu de l'historique du procès
À ce jour, le PRF a financé et coordonné quatre essais cliniques. La PRF est et a toujours été responsable de tous les frais des essais, y compris les tests, les déplacements, la nourriture, l'hébergement, les traducteurs et le personnel. Chaque nouvel essai est plus coûteux que le précédent, car de plus en plus d'enfants s'inscrivent pour avoir une chance de vivre plus longtemps et en meilleure santé.
Détails sur les procès antérieurs
Le projet #1, qui impliquait un seul médicament, le lonafarnib, a débuté en 2007 et s'est avéré efficace. Découvrez tout sur cette découverte historique du traitement ici.
#2, la partie « faisabilité » de l’« essai triple » impliquait 3 médicaments : le lonafarnib, la pravastatine et le zolédronate. Ce « mini-essai » de phase 1 d’un mois a eu lieu en mars 2009 pour déterminer si l’ajout de 2 médicaments supplémentaires au traitement par le lonafarnib était sans danger pour une population plus large (ce qui était le cas).
L’essai #3, le « Triple Trial », était une continuation de l’essai de faisabilité et une étude de phase 2 qui a débuté en août 2009. Son protocole a changé au cours des cinq années suivantes, revenant au seul lonafarnib et réouvrant les inscriptions pour que davantage d’enfants puissent participer. Lire la suite ici.
L'essai #4 porte sur deux médicaments, le lonafarnib et l'évérolimus. La phase 1, visant à déterminer le dosage sûr et approprié de l'évérolimus, a débuté en avril 2016 et s'est achevée avec succès en juin 2017. La phase 2, qui a testé l'efficacité de l'association de deux médicaments, a débuté en juillet 2017 et s'est achevée en avril 2022. L'extension de monothérapie de cet essai se poursuit aujourd'hui.
7 mai 2007 : Le début du tout premier essai clinique du médicament contre la progéria marque un moment historique dans l'histoire de la recherche sur la progéria !
En 2006, les chercheurs ont identifié un traitement médicamenteux potentiel pour les enfants atteints de progéria, appelés FTI. Pour la première fois, nous avions devant nous un traitement possible pour les enfants atteints de progéria. Des moments passionnants ! L'essai clinique du médicament Progeria a débuté le 7 mai 2007 avec l'arrivée de deux enfants – Meghan et Megan – au Boston Children's Hospital de Boston, dans le Massachusetts, pour leur première visite sur sept sur une période de deux ans. Lors de cette première visite, elles ont subi des tests approfondis et reçu leurs premières doses du médicament. En moyenne, deux familles se sont rendues à Boston chaque semaine par la suite, jusqu'en décembre 2009, période pendant laquelle l'équipe de l'essai a analysé les milliers d'éléments de données (chaque enfant a subi plus de 100 tests par visite !) et a demandé la publication des résultats.
« Je ne connais aucune autre maladie génétique rare qui soit passée de la découverte du gène à l’essai clinique en moins de quatre ans – un témoignage phénoménal du travail acharné de la Progeria Research Foundation. »
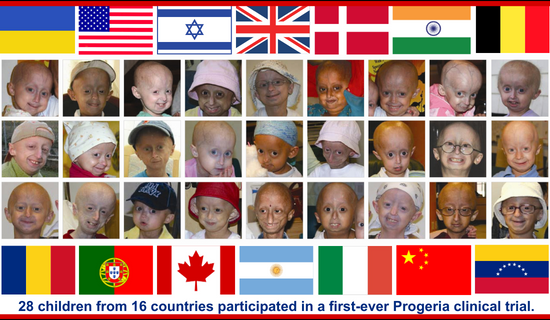
Vingt-huit (28) enfants de seize pays ont participé à l'essai, âgés de 3 à 15 ans. Les enfants sont retournés à l'hôpital pour enfants de Boston tous les quatre mois pour subir des tests et recevoir de nouveaux médicaments. Ils sont restés à Boston pendant 4 à 8 jours à chaque visite. À la maison, leurs médecins ont surveillé de près les enfants et ont soumis des rapports de santé périodiques à l'équipe de recherche de Boston. Pendant toute la durée de l'essai, en moyenne 2 enfants par semaine se sont rendus à Boston pour participer.
Qui, Où, Quand, Comment et Combien…
Les trois premiers essais cliniques ont été dirigés par le Dr Mark Kieran, PhD, Directeur, Neuro-oncologie médicale pédiatrique, Dana-Farber Cancer Institute et Children's Hospital Boston ; professeur adjoint, départements de pédiatrie et d'hématologie/oncologie, Harvard Medical School. Le Dr Kieran est un oncologue pédiatrique possédant une vaste expérience du médicament à l'étude (farnésyltransférase, ou FTI) chez les enfants. En 2017, il a quitté son poste chez Dana Farber pour travailler dans le secteur privé. Les coprésidents étaient Monica Kleinman, MD, directrice de l'unité de soins intensifs médico-chirurgicaux, associée principale en médecine de soins intensifs au BCH, professeur adjoint à la Harvard Medical School ; et Leslie Gordon, MD, PhD, directrice médicale du PRF, chargée de cours au BCH et à la Harvard Medical School, professeur de pédiatrie au Hasbro Children's Hospital et à la Brown University à Providence, RI. Le Dr Kleinman a assumé le rôle principal de chercheur principal.
Les essais cliniques sont le fruit d'un effort collaboratif impliquant des médecins du Boston Children's Hospital, du Dana-Farber Cancer Institute et du Brigham and Women's Hospital., toutes les institutions de l'Université Harvard. De plus, des médecins et des scientifiques de la Warren Alpert Medical School de l'Université Brown et du NIH ont contribué au succès de ce premier essai et des suivants.
Comment en sommes-nous arrivés là ?
En 2003, l'équipe de recherche collaborative de la Fondation de recherche sur la progéria découvert le gène de la progéria. Cette découverte a non seulement permis de mieux comprendre la progéria, mais les scientifiques savent désormais que l’étude de la progéria peut nous aider à en apprendre davantage sur les maladies cardiaques et le processus normal de vieillissement qui nous affecte tous. Depuis la découverte du gène, le soutien des chercheurs, des cliniciens, des familles d’enfants atteints de progéria et des personnes comme VOUS nous a amenés à un autre carrefour dans la recherche d’un traitement. Les chercheurs ont commencé une étude intensive de cette protéine ennemie appelée progérine, et en 2006, ils ont identifié un traitement médicamenteux potentiel pour les enfants atteints de progéria, appelé inhibiteurs de la farnésyltransférase (FTI), et ont mené des études en laboratoire qui ont soutenu un essai sur l'homme avec le médicament. Le FTI choisi a été initialement fourni par Merck et appelé lonafarnib. Cliquez ici pour plus de détails sur la recherche.
Pourquoi les chercheurs pensaient-ils que ce médicament fonctionnerait contre la progéria ?
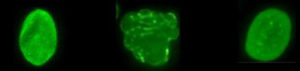
Cellule normale, cellule Progeria, cellule Progeria après traitement avec FTI.
La protéine que nous pensons responsable de la progéria s’appelle la progérine. Pour bloquer la fonction cellulaire normale et provoquer la progéria, une molécule appelée « groupe farnésyle » doit être attachée à la protéine progérine. Les FTI agissent en bloquant (inhibant) la fixation du groupe farnésyle sur la progérine. Ainsi, si le médicament FTI peut bloquer la fixation du groupe farnésyle sur la progérine chez les enfants atteints de progéria, la progérine pourrait alors être « paralysée » et la progéria améliorée. Cliquez ici pour plus d'informations sur les FTI.
Comment le PRF a-t-il financé le procès ?
Grâce au soutien de milliers de personnes, nous avons pu réunir tous les fonds nécessaires pour couvrir les frais du procès. Nous exprimons notre plus sincère gratitude à tous ceux qui ont consacré leur temps, leurs talents et leur argent à rendre possible cette incroyable réussite, et bien sûr à toutes les familles courageuses qui y ont participé.
Le lonafarnib de FTI est désormais un traitement éprouvé contre la progéria.
En 2012, les résultats de l’étude ont été publiés, démontrant que chaque enfant a connu une amélioration dans un ou plusieurs domaines, y compris le système cardiovasculaire vital. En mai 2014, une étude a montré qu’un ou plusieurs des 3 médicaments – dont le lonafarnib – testés dans le cadre d’essais cliniques financés par le PRF prolongeaient la durée de vie ; on ne savait pas quel médicament avait cet impact positif sur la vie. Cependant, en avril 2018, une étude publiée dans Journal de l'Association médicale américaine (JAMA) il a été rapporté que le lonafarnib seul prolongeait la survie des enfants atteints de progéria d'au moins 1,6 an. Cliquez ici pour plus de détails sur l'étude historique de découverte de traitement de 2012, ici pour plus de détails sur les résultats de 2014, et ici pour plus de détails sur l’étude de 2018.
« TOUT LE MONDE a été si merveilleux. Pour nous, vous êtes TOUS ENVOYÉS PAR DIEU et nous APPRÉCIONS tout ce que vous faites pour ces petits anges. Notre famille est tellement submergée par l'excitation et toutes sortes d'émotions à l'idée du voyage d'Adalia à Boston ce week-end, que je ne peux même pas commencer à écrire les mots pour exprimer ce que nous ressentons. »
« Ce nouveau médicament pour Zach nous redonne l’espoir que son cœur sera plus fort, son sourire plus éclatant et sa vie plus longue. Ce nouveau médicament est une réponse à nos prières. Merci à tous ceux qui ont participé à la PRF et qui ont rendu cela possible… les médecins, les chercheurs et le personnel. Vous êtes nos héros ! »
« Au nom de Cam et de notre famille, merci beaucoup à tous les membres de PRF pour tout ce que vous avez fait ! Sans vous, nous serions perdus dans un monde de confusion et de chagrin. Au lieu de cela, nous vivons dans un monde d’espoir et de détermination. Merci encore et encore ! Avec beaucoup d’amour et de respect. »

Toujours en marche vers l'avant : l'essai clinique du triple médicament contre la progéria débute en août 2009
Résumé:
Les chercheurs ont identifié deux médicaments supplémentaires qui, utilisés en association avec le médicament FTI actuellement testé (lonafarnib), pourraient constituer un traitement encore plus efficace pour les enfants atteints de progéria que le FTI seul. La pravastatine et le zolédronate ont été ajoutés au traitement actuel, le lonafarnib. Cet essai beaucoup plus vaste a porté sur 45 enfants de 24 pays différents !
Stratégie:
Ces trois médicaments ciblent des points différents le long de la voie conduisant à la production de la progérine, responsable de la maladie. Dans le cadre d'études de laboratoire passionnantes présentées par le Dr Carlos Lopez-Otin d'Espagne lors de l'atelier scientifique 2007 de la Progeria Research Foundation, les deux nouveaux médicaments ont amélioré la maladie dans les cellules progéria et prolongé la durée de vie dans les modèles murins de progéria.
But:
Si les trois médicaments administrés dans cet essai peuvent bloquer efficacement cette fixation du groupe farnésyl, alors la progérine pourrait être « paralysée » et la progéria pourrait être améliorée encore plus qu’avec le lonafarnib seul. On espère que les médicaments fonctionneront comme des partenaires, pour se compléter mutuellement, de sorte que la protéine progérine soit davantage affectée par la combinaison des trois médicaments.
L'essai de faisabilité :
L’équipe a mené un mini-essai sur cinq enfants atteints de progéria. L’essai de « faisabilité » d’un mois visait à déterminer si la combinaison de trois médicaments serait bien tolérée, avant de se lancer dans un essai international de plus grande envergure. Les effets secondaires se sont révélés acceptables et l’équipe a procédé à un essai d’efficacité de plus grande envergure.
L'essai d'efficacité :
45 enfants ont participé à cet essai, originaires de 24 pays et parlant 17 langues. Cela comprend les enfants qui ont participé à l'essai FTI uniquement, les participants à l'essai de faisabilité et d'autres enfants qui étaient soit trop jeunes pour participer au premier essai, soit des enfants que nous avons découverts au cours du premier essai clinique (après la fin du recrutement). Les enfants inscrits à l'essai FTI uniquement ont eu la possibilité de s'inscrire à l'essai triple lors de leur dernière visite pour l'essai en cours. Cela a permis à ces enfants de continuer à prendre FTI sans manquer aucune dose.
Aperçu des médicaments à l'essai
Pravastatine (commercialisé sous le nom de Pravachol ou Selektine) fait partie de la classe des médicaments appelés statines. Il est généralement utilisé pour réduire le cholestérol et prévenir les maladies cardiovasculaires.
Acide zolédronique est un bisphosphonate, généralement utilisé comme médicament osseux pour améliorer l’ostéoporose et pour prévenir les fractures squelettiques chez les personnes souffrant de certaines formes de cancer.
Lonafarnib est un FTI (Inhibiteur de la farnésyltransférase), un médicament qui peut inverser une anomalie dans les cellules Progeria en laboratoire, et qui a amélioré la maladie chez les souris Progeria.
Les trois médicaments bloquent la production de la molécule de farnésyle nécessaire à la progérine pour créer la maladie de Progeria.
* «Un traitement combiné à base de statines et d'aminobisphosphonates prolonge la longévité dans un modèle murin de vieillissement prématuré humain", par Ignacio Varela, Sandrine Pereira, Alejandro P. Ugalde, Claire L. Navarro, María F. Suarez, Pierre Cau, Juan Cadinanos, Fernando G. Osorio, Nicolas Foray, Juan Cobo, Felix de Carlos, Nicolas Levy, Jose Le député Freije et Carlos Lopez-Otan. Médecine naturelle, 2008. 14(7) : p. 767-72.
En juillet un étude ** a été publié et n'a montré aucune amélioration significative par rapport à la monothérapie par lonafarnib. **Gordon, et. al., Essai clinique des inhibiteurs de la farnésylation des protéines lonafarnib, pravastatine et acide zolédronique chez les enfants atteints du syndrome de Hutchinson-Gilford-Progeria, Circulation, 10.1161/CIRCULATIONAHA.116.022188
Cependant, le « Triple essai » a été prolongé au-delà de sa durée initiale de 2 à 3 ans et a été élargi pour inclure jusqu’à 80 enfants, afin que chaque enfant puisse avoir accès au lonafarnib seul, car nous savons que ce médicament les aide. Habituellement, les essais cliniques suivent leur cours et les patients sont privés de tous les médicaments jusqu’à l’approbation de la FDA, ce qui peut prendre des années. La PRF a veillé à ce que les enfants continuent de prendre le seul traitement connu, tandis qu’elle et ses partenaires de recherche continuent d’explorer d’autres options de traitement (comme l’évérolimus qui est actuellement testé).
L'ajout d'un plus récent Médicament : Everolimus
L’évérolimus est une forme de rapamycine, un médicament qui pourrait être administré plus facilement aux enfants atteints de progéria, car il nécessite moins de prises de sang pour mesurer les concentrations du médicament. Alors que le lonafarnib peut bloquer le développement de la progérine toxique, la rapamycine semble permettre aux cellules d’éliminer plus rapidement la progérine. Ainsi, la rapamycine ciblant une voie différente de celle du lonafarnib, la combinaison pourrait s’avérer être un « coup double » contre la progéria – et, espérons-le, un meilleur traitement que le lonafarnib seul.
La science derrière l’ajout de ce deuxième médicament
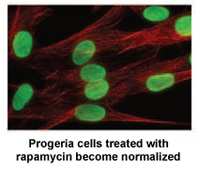
Rapamycin est un médicament approuvé par la FDA qui a déjà montré qu'il prolongeait la vie des modèles de souris non atteintes de la progéria. Une étude* menée par des chercheurs du NIH à Bethesda, dans le Maryland, et du Massachusetts General Hospital à Boston démontre que la rapamycine diminue la quantité de la protéine progérine responsable de la maladie de 50%, améliore la forme nucléaire anormale et prolonge la durée de vie des cellules de la progéria en laboratoire.
La rapamycine est connue pour ses propriétés anti-âge chez la souris. Ces résultats font partie d’une liste croissante d’études qui contribuent à valider la théorie selon laquelle la découverte d’un remède contre la progéria pourrait également bénéficier à l’ensemble de la population vieillissante.
* K. Cao, J. J. Graziotto, C. D. Blair, J. R. Mazzulli, M. R. Erdos, D. Krainc, F. S. Collins, « La rapamycine inverse les phénotypes cellulaires et améliore la clairance des protéines mutantes dans les cellules atteintes du syndrome de Hutchinson-Gilford progéria. » Sci. Transl. Med. 3, 89ra58 (2011).
La Fondation de recherche sur la progéria a fourni des cellules pour ce projet à partir du Banque de cellules et de tissus PRF et a aidé à financer la recherche grâce à notre programme de subventions – une preuve supplémentaire que les programmes de recherche du PRF sont essentiels aux progrès vers la guérison.
Cet essai portant sur deux médicaments est le fruit d'une collaboration qui s'appuie sur les connaissances acquises lors des précédents essais cliniques du PRF. Les enfants ont été suivis par pratiquement la même équipe de médecins du Boston Children's Hospital et du Brigham and Women's Hospital, qui possèdent tous désormais une expertise reconnue mondialement dans le domaine de la progéria ainsi que dans les médicaments impliqués.
Soixante enfants de 27 pays ont été recrutés dans cette phase à deux médicaments. Les données de la partie de l'essai à deux médicaments sont en cours d'analyse et les résultats sont en cours de formulation et de rédaction en vue d'une publication dans une revue scientifique à comité de lecture.
Notre quête du remède continue…
Nos travaux sur les thérapies génétiques avancent à grands pas ! Études sur la thérapie par ARN et l'édition génétique de l'ADN ont montré une vaste amélioration de la durée de vie des souris atteintes de Progeria. PRF continue d’investir des fonds substantiels dans leur développement, avec l’espoir que ces efforts de recherche conduire à des essais cliniques et, finalement, au remède.
Ces thérapies de pointe ont énorme potentiel! Avec votre aide, PRF peut continuer à progresser le plus rapidement possible vers les traitements les plus efficaces et la guérison.


