Este primeiro envio é o resultado de doze anos de dados de pesquisa e quatro ensaios clínicos financiados pela PRF em parceria com a Brown University e o Boston Children's Hospital, e foi possível graças às crianças corajosas e suas famílias, assim como a VOCÊ, a maravilhosa comunidade de doadores da PRF.
Você pode ler mais sobre esta notícia emocionante aqui.
A Eiger BioPharmaceuticals enviará partes concluídas do requerimento para revisão da FDA de forma contínua, com planos de finalizar o envio no primeiro trimestre do ano novo. A aprovação permitirá que essas crianças e jovens adultos acessem o lonafarnib – que demonstrou dar a eles corações mais fortes e vidas mais longas – por prescrição, em vez de por meio de nossos ensaios clínicos, nos EUA e possivelmente em outros países também.
Que maneira positiva de terminar 2019 e começar o Ano Novo com força! Trabalhamos incansavelmente para causar um impacto significativo na vida de crianças e jovens adultos com Progéria, e esta submissão nos aproxima desse objetivo.
OBRIGADO A TODOS por apoiar a pesquisa que não apenas nos trouxe a esse ponto crucial, mas também nos permite continuar trabalhando para descobrir novos medicamentos que acabarão curando essas crianças extraordinárias.
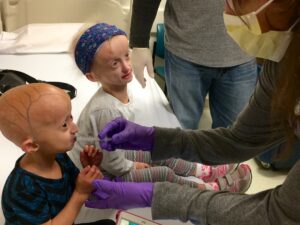
Zoey e Carly recebendo tratamento com lonafarnib durante sua última visita de teste clínico em Boston.