Эта первая в истории подача заявки является кульминацией двенадцати лет исследований и четырех клинических испытаний, финансируемых PRF в партнерстве с Университетом Брауна и Детской больницей Бостона, и стала возможной благодаря мужественным детям и их семьям, а также ВАМ – замечательному сообществу доноров PRF.
Вы можете прочитать больше об этой захватывающей новости здесь.
Eiger BioPharmaceuticals будет подавать завершенные части заявки на рассмотрение FDA на постоянной основе, с планами завершить подачу в первом квартале нового года. Одобрение позволит этим детям и молодым людям получить доступ к лонафарнибу, который, как было показано, дает им более сильные сердца и более долгую жизнь, по рецепту, а не через наши клинические испытания, в США и, возможно, в других странах.
Какой позитивный способ завершить 2019 год и начать Новый год с новыми силами! Мы неустанно трудились, чтобы оказать значимое влияние на жизни детей и молодых людей, страдающих прогерией, и эта работа приближает нас к этой цели.
СПАСИБО ВСЕМ за поддержку исследования, которое не только привело нас к этой поворотной точке, но и позволяет нам продолжать работу по открытию новых препаратов, которые в конечном итоге вылечат этих необыкновенных детей.
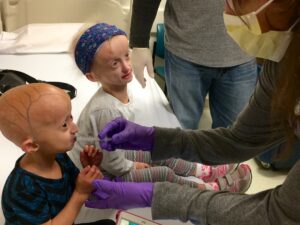
Зои и Карли получают лечение лонафарнибом во время своего последнего визита в Бостон с клиническими испытаниями.