Це перше в історії подання є кульмінацією дванадцятьох років досліджень і чотирьох клінічних випробувань, фінансованих PRF у партнерстві з Університетом Брауна та Бостонською дитячою лікарнею, що стало можливим завдяки сміливим дітям та їхнім родинам, а також ВАМ – чудовій спільноті PRF. донорів.
Ви можете прочитати більше про цю захоплюючу новину тут.
Eiger BioPharmaceuticals постійно подаватиме завершені частини заявки на розгляд FDA, плануючи завершити подання в першому кварталі нового року. Схвалення дасть змогу цим дітям і молодим дорослим отримати доступ до лонафарнібу – який, як було показано, зміцнює їх серце і продовжує життя – за рецептом, а не через наші клінічні випробування, у США та, можливо, також в інших країнах.
Який позитивний спосіб завершити 2019 рік і розпочати Новий рік із силою! Ми невтомно працювали над тим, щоб суттєво вплинути на життя дітей і молодих людей, хворих на прогерію, і ця заява наближає нас до цієї мети.
ДЯКУЮ ВАМ ВСІМ за підтримку дослідження, яке не тільки привело нас до цього ключового моменту, але й дозволяє нам продовжувати роботу над відкриттям нових ліків, які зрештою вилікують цих надзвичайних дітей.
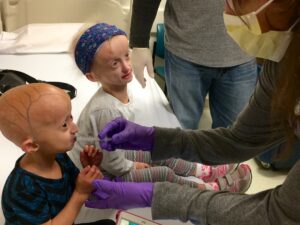
Зої та Карлі отримують лікування лонафарнібом під час останнього візиту до Бостона для проведення клінічних випробувань.